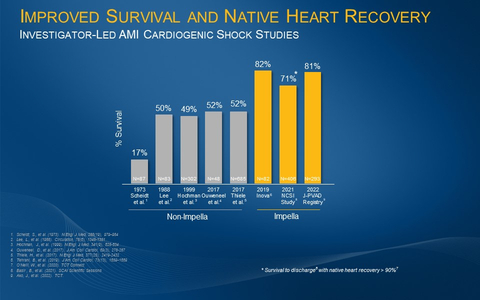
Eine große, multizentrische und von mehreren Gesellschaften durchgeführte Studie mit Patienten, die Unterstützung von Impella erhielten, ermittelt dass die Überlebensrate bei einem kardiogenen Schock nach 30 Tagen AMI bei 81 % liegt
Eine große, multizentrische und von mehreren Gesellschaften durchgeführte Studie mit Patienten, die Unterstützung von Impella erhielten, ermittelt dass die Überlebensrate bei einem kardiogenen Schock nach 30 Tagen AMI bei 81 % liegt
BOSTON--(BUSINESS WIRE)--Die Ergebnisse einer dreijährigen, von Forschern geleiteten Studie aller mit Impella unterstützten Patienten, die in 109 Krankenhäusern in Japan (n=1.344) behandelt wurden, zeigen 30-tägige Überlebensraten von 81 Prozent bei Patienten mit AMI-bedingtem kardiogenem Schock (AMICS). Die Studie ist eine Aktualisierung einer 2020 durchgeführten Zwischenanalyse und wurde auf der Transcatheter Cardiovascular Therapeutics (TCT) Konferenz 2022 in Boston vorgestellt.
Im Rahmen der Analyse wurden 293 aufeinander folgende mit Impella unterstützte AMICS-Patienten im J-PVAD-Register untersucht. Dieses Register wird von 10 japanischen Fachgesellschaften geführt, darunter die Japanische Kreislaufgesellschaft (JCS). Die Ergebnisse zeigten eine Überlebensrate von 81 Prozent nach 30 Tagen. Historisch gesehen liegen die Überlebensraten im Falle von kardiogenem Schock ohne Impella bei rund 50 Prozent.
„Die Ergebnisse dieser Studie belegen, dass beim Einsatz von Impella und empfohlenen Behandlungsmethoden eine Herzerholung und eine mehr als 80-prozentige Überlebensrate von Patienten mit AMI-bezogenem kardiogenem Schock möglich sind“, so der leitende Prüfarzt Dr. Junya Ako, interventioneller Kardiologe und Vorsitzender der Abteilung für kardiovaskuläre Medizin am Kitasato University Hospital in Kanagawa.
Diese Ergebnisse stehen im Einklang mit anderen veröffentlichten, von Wissenschaftlern durchgeführten Studien, wie etwa die National Cardiogenic Shock Initiative Study (NCSI) und die Inova-Studie von Tehrani et al., die beim Einsatz von Impella und empfohlenen Behandlungsmethoden, darunter die Platzierung von Impella vor einer perkutanen Koronarintervention (PCI), signifikant höhere Überlebensraten nachgewiesen haben (siehe Abb. 1).
Die Daten des J-PVAD werden überwacht und mit der japanischen Behörde für Arzneimittel und Medizinprodukte (PMDA) geteilt.
ÜBER IMPELLA HERZPUMPEN
Impella 2.5, Impella CP®, Impella CP mit SmartAssist, Impella 5.0®, Impella LD®, und Impella 5.5® mit SmartAssist® sind von der US-amerikanischen FDA zur Behandlung von Herzinfarkt- oder Kardiomyopathie-Patienten mit kardiogenem Schock zugelassen. Diese einzigartigen Herzpumpen ermöglichen eine Wiederherstellung der nativen Herzfunktion, sodass die Patienten mit ihrem eigenen Herzen nach Hause entlassen werden können.
ÜBER ABIOMED
Abiomed (Nasdaq: ABMD) mit Sitz in Danvers, Massachusetts (USA), ist ein führender Anbieter von Medizintechnik zur Kreislaufunterstützung und Oxygenierung. Unsere Produkte entlasten das Herz und unterstützen seine Erholung durch die Verbesserung des Blutflusses und/oder stellen eine ausreichende Sauerstoffversorgung bei Patienten mit Atemwegsversagen sicher. Weitere Informationen erhalten Sie unter https://protect-us.mimecast.com/s/_xB7CR6wLZHNwLWVfXFbsV?domain=abiomed.com.
ZUKUNFTSGERICHTETE AUSSAGEN
Zukunftsgerichtete Aussagen unterliegen Risiken und Unwägbarkeiten, wie sie in den periodischen Berichten von Abiomed, die bei der Securities and Exchange Commission hinterlegt sind, beschrieben werden. Die tatsächlichen Ergebnisse können erheblich von den erwarteten Ergebnissen abweichen.
Die Ausgangssprache, in der der Originaltext veröffentlicht wird, ist die offizielle und autorisierte Version. Übersetzungen werden zur besseren Verständigung mitgeliefert. Nur die Sprachversion, die im Original veröffentlicht wurde, ist rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen Sprachversion der Veröffentlichung ab.
Contacts
Weitere Informationen:
Medienkontakt:
Jenny Leary
Associate Director, U.S. Communications
+1 (978) 882-8491
jleary@abiomed.com
Investorenkontakt:
Todd Trapp
Executive Vice President und Chief Financial Officer
+1 (978) 646-1680
ttrapp@abiomed.com