Cybin anuncia datos provisionales positivos sin precedentes de fase 2 para CYB003 en el trastorno depresivo mayor que cumplen el criterio de valoración de eficacia primaria con mejoras rápidas y significativas de los síntomas de depresión tras una...
Cybin anuncia datos provisionales positivos sin precedentes de fase 2 para CYB003 en el trastorno depresivo mayor que cumplen el criterio de valoración de eficacia primaria con mejoras rápidas y significativas de los síntomas de depresión tras una...
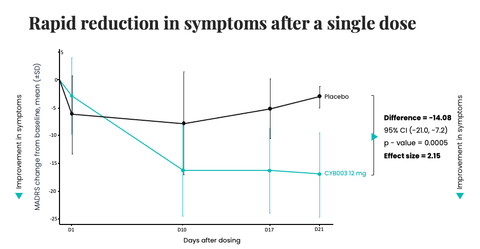
- La lectura provisional muestra una reducción rápida, robusta y clínicamente significativa de los síntomas de depresión tres semanas después de una dosis única de 12 mg, con una reducción media sin precedentes de -14 puntos en la puntuación de la Escala de Calificación de la Depresión de Montgomery-Asberg ("MADRS") con respecto al valor basal entre CYB003 (12 mg) versus placebo (p= 0,0005) -
- A modo de comparación, los datos agrupados de 232 estudios industriales sobre los antidepresivos de referencia actuales, los inhibidores selectivos de la recaptación de serotonina (ISRS), presentados a la FDA (Stone et al, 2022) muestran una mejora media de 1,82 puntos versus placebo -
- Respuesta y remisión sólidas tres semanas después de la dosis única, con un 53,3% de pacientes con respuesta y un 20% de pacientes en remisión (que ya no cumplen la definición clínica de depresión) versus 0% para el placebo -
- Perfil de seguridad y tolerabilidad favorable, sin acontecimientos adversos graves relacionados con el tratamiento en la dosis de 12 mg -
- Los datos completos están previstos para el cuarto trimestre de 2023 -
- La empresa celebrará una conferencia telefónica para comentar los resultados provisionales de CYB003 el miércoles 1 de noviembre de 2023 a las 11:00 horas ET –
Este comunicado de prensa constituye un "comunicado de prensa designado" a los efectos de los suplementos de prospecto de Cybin, cada uno de ellos de fecha 23 de agosto de 2023, a su prospecto base abreviado de fecha 17 de agosto de 2023.
TORONTO--(BUSINESS WIRE)--
Cybin anuncia datos provisionales positivos sin precedentes de fase 2 para CYB003 en el trastorno depresivo mayor que cumplen el criterio de valoración de eficacia primaria con mejoras rápidas y significativas de los síntomas de depresión tras una sola dosis
Cybin Inc. (NYSE American:CYBN) (NEO:CYBN) ("Cybin" o la "Compañía"), una compañía biofarmacéutica en fase clínica, centrada en revolucionar la atención sanitaria mental mediante el desarrollo de nuevas e innovadoras opciones de tratamiento psicodélico de nueva generación, ha anunciado hoy los resultados provisionales de Fase 2 de CYB003, su análogo de psilocibina deuterada patentado, que demuestran una reducción rápida, sólida y estadísticamente significativa de los síntomas de depresión tres semanas después de una única dosis de 12 mg en comparación con placebo.
El comunicado en el idioma original es la versión oficial y autorizada del mismo. Esta traducción es solamente un medio de ayuda y deberá ser comparada con el texto en idioma original, que es la única versión del texto que tendrá validez legal.
Contacts
Inversores y medios de comunicación:
Gabriel Fahel
Director de Asuntos Jurídicos
Cybin Inc.
1-866-292-4601
irteam@cybin.com – o – media@cybin.com