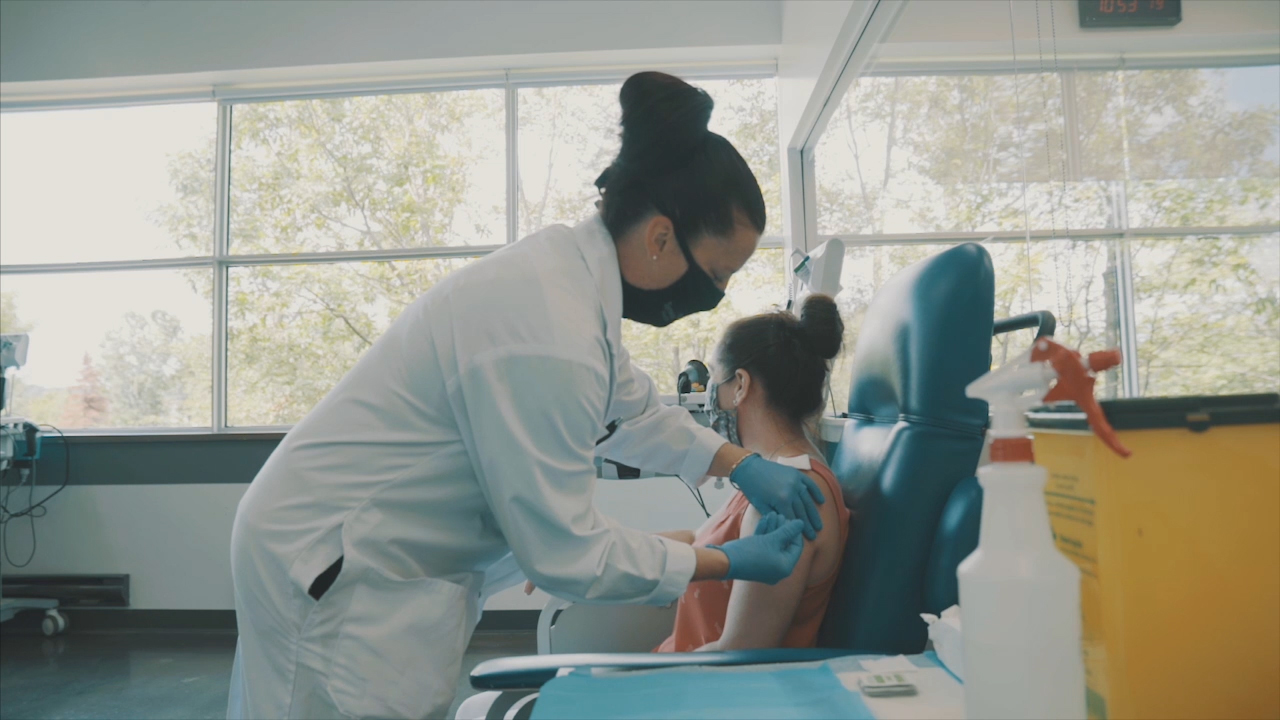
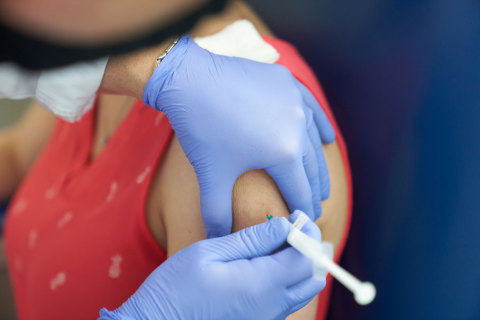
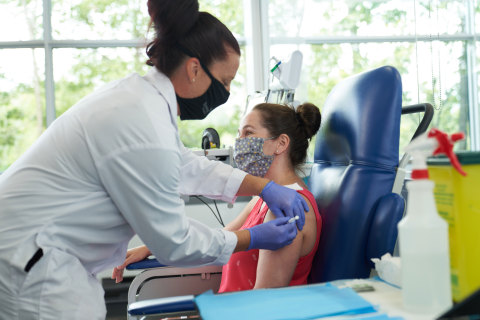
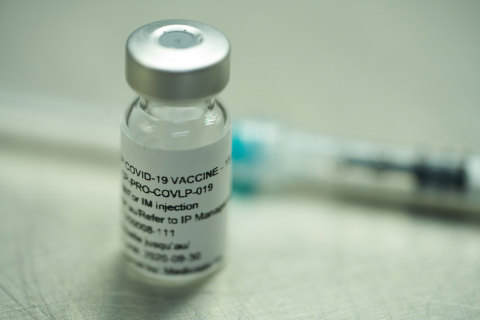QUEBEC, Kanada--(BUSINESS WIRE)--Medicago, ein biopharmazeutisches Unternehmen mit Sitz in Quebec, hat gestern die klinischen Studien der Phase 1 für seinen aus Pflanzen gewonnenen COVID-19-Impfstoffkandidaten begonnen und gesunden menschlichen Probanden die ersten Dosen verabreicht. Medicago plant außerdem eine Phase-2/3-Studie, die im Oktober dieses Jahres beginnen soll.
„Wir freuen uns sehr über den Start der Phase-1-Studie für unseren COVID-19-Impfstoffkandidaten und sehen den Ergebnissen zur Sicherheit und Immunogenität, die im Oktober vorliegen werden, erwartungsvoll entgegen“, so Nathalie Landry, Executive Vice-President, Scientific and Medical Affairs, Medicago. „Unsere Fortschritte unterstreichen das Potenzial der einzigartigen pflanzenbasierten Impfstofftechnologie von Medicago.“
Bei der klinischen Phase-1-Studie handelt es sich um eine randomisierte, partiell verblindete Studie an 180 gesunden Probanden männlichen und weiblichen Geschlechts im Alter von 18 bis 55 Jahren. Untersucht werden Dosierungen von 3,75, 7,5 und 15 Mikrogramm des rekombinanten CoVLP-Impfstoffkandidaten (Coronavirus Virus-Like Particle) allein oder in Verbindung mit einem Adjuvans als Teil eines Prime-Boost-Schemas. Medicago wird seinen Impfstoffkandidaten mit zwei Adjuvanzien separat testen: der proprietären GSK-Pandemie-Adjuvans-Technologie und mit Dynavax CpG 1018™. In einer Pandemiesituation kann ein Adjuvans von besonderer Bedeutung sein, da es die Immunantwort verstärken und die Menge des benötigten Antigens je Dosis verringern kann, sodass mehr Impfstoffdosen hergestellt werden und somit zum Schutz einer möglichst großen Zahl von Menschen beitragen können.
Die innovative Plattform und die pflanzenbasierte Herstellungstechnologie von Medicago diversifizieren den Pool der in der Entwicklung befindlichen COVID-19-Impfstoffe.
„Der Aufbau einer ausreichenden Versorgung an COVID-19-Impfstoffen innerhalb eines Jahres ist eine Herausforderung, die mehrere Ansätze mit unterschiedlichen Technologien erfordern wird“, berichtet Dr. Bruce Clark, Präsident und CEO bei Medicago. „Unsere bewährte pflanzenbasierte Technologie kann einen wichtigen Beitrag zur kollektiven Bewältigung dieser Krise des Gesundheitswesens leisten.“
Medicago rechnet damit, bis Ende 2021 etwa 100 Millionen Dosen herstellen zu können. Bis Ende 2023 wird der Bau des umfangreichen Medicago-Produktionsstandorts in Quebec (Kanada) abgeschlossen sein. Es wird erwartet, dass diese kommerzielle Anlage eine ausreichende Kapazität für bis zu 1 Milliarde Dosen des COVID-19-Impfstoffs pro Jahr bereitstellen wird.
Medicago ist das einzige Unternehmen mit pflanzenbasierter Herstellungstechnologie, das klinische Studien der Phase III (zum vierwertigen VLP-Influenza-Impfstoffkandidaten) und pandemische klinische Studien der Phase II (zum H1N1-Pandemie-Impfstoffkandidaten) abgeschlossen hat. Der erste Zulassungsantrag des Unternehmens für seinen saisonalen rekombinanten vierwertigen VLP-Impfstoff zur aktiven Immunisierung gegen Influenza bei Erwachsenen (18-64 Jahre) wird derzeit von der kanadischen Gesundheitsbehörde Health Canada geprüft, nachdem robuste klinische Sicherheits- und Wirksamkeitsstudien an über 25.000 Probanden abgeschlossen wurden.
Neben seiner Erfahrung in der klinischen Entwicklung hat Medicago auch seine Fähigkeit unter Beweis gestellt, in kurzer Zeit große Volumen an Impfstoffen herzustellen. Im Jahr 2012 produzierte Medicago innerhalb nur eines Monats 10 Millionen Dosen einwertiger Impfstoffe gegen die pandemische Influenza H1N1 für die Defense Advanced Research Projects Agency (DARPA), die zum US-Verteidigungsministeriums gehört.
Die pflanzenbasierte Plattform von Medicago
Bei der Entwicklung von Protein-Therapeutika und Impfstoffen setzt das Unternehmen seine unternehmenseigene pflanzenbasierte Technologie ein. Im Gegensatz zur herkömmlichen Entwicklung von Impfstoffen verwendet Medicago keine tierischen Produkte oder Lebendviren. Stattdessen verwendet das Unternehmen virusähnliche Partikel (VLP), die die Form und Größe eines Virus imitieren, sodass der Körper sie erkennt und eine Immunreaktion auslöst, die nicht auf einer Infektion basiert. Daten aus klinischen Studien legen nahe, dass VLPs über einen multimodalen Wirkungsmechanismus verfügen, der sich von inaktivierten Impfstoffen unterscheidet und beide Arme des Immunsystems – Antikörper und zellvermittelte Immunreaktion – aktiviert.
Die proprietäre Technologie von Medicago ist schnell, vielseitig und skalierbar. Sobald die Gensequenz eines Virus vorliegt, kann Medicago in nur wenigen Wochen einen klinischen Impfstoffkandidaten entwickeln. Die rekombinante Technologie ermöglicht die Herstellung eines Impfstoffs, der genau auf die im Umlauf befindlichen Stämme, wie beispielsweise bei der saisonalen Grippe, abgestimmt ist. Da sich die Technologie mühelos skalieren lässt, kann Medicago das Produktionsvolumen ganz einfach durch Erhöhung der Anzahl verwendeter Pflanzen steigern.
Standorte
Medicago ist in Quebec (Kanada) niedergelassen und plant die Herstellung von COVID-19-Impfstoffen in Durham im US-Bundesstaat North Carolina sowie in seiner Pilotanlage in Quebec. Eine neue, hochmoderne Produktionsstätte, die zurzeit in Quebec errichtet wird, soll über eine jährliche Kapazität von bis zu 1 Milliarde COVID-19-Impfungen verfügen.
Über Medicago
Medicago ist ein biopharmazeutisches Unternehmen mit Hauptsitz in Quebec (Kanada) sowie Produktionsstandorten in Quebec und Durham, North Carolina, USA. Das Ziel von Medicago besteht darin, die weltweiten Behandlungsergebnisse mithilfe von innovativen pflanzenbasierten Technologien zu verbessern, um schneller auf neu entstehende globale Herausforderungen für Gesundheitssysteme reagieren zu können. Medicago strebt an, die Entwicklung von Therapeutika für lebensbedrohliche Krankheiten weltweit voranzubringen.
Nähere Informationen unter: www.medicago.com
Die Ausgangssprache, in der der Originaltext veröffentlicht wird, ist die offizielle und autorisierte Version. Übersetzungen werden zur besseren Verständigung mitgeliefert. Nur die Sprachversion, die im Original veröffentlicht wurde, ist rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen Sprachversion der Veröffentlichung ab.